НФОрУГАЁ 15РЯ, ФкЗЮГЊ19АЁ РчШЎЛъЕЧАэ ЕЖАЈРЬ РЏЧрЧЯДТ АшР§РЬ ДйАЁПШПЁ ЕћЖѓ K-ЙцПЊ НУНКХлРЧ ЧйНЩРЮ ФкЗЮГЊ19 СјДмНУОрРЧ ЧуАЁ‧НЩЛч ЛѓШВ ЕюПЁ ДыЧб ЧіШВРЛ ЙпЧЅЧпДй.
ЧіРч ФкЗЮГЊ19 СјДм ЕюРЛ РЇЧи БЙГЛ ЛчПыРЬ АЁДЩЧб СІЧАРК ЁуШЎСј АЫЛчПы БфБоЛчПыНТРЮ СІЧА 7АГ ЁуРРБо МБКАПы БфБоЛчПыНТРЮ СІЧА 9АГ ЁуСЄНФЧуАЁ СІЧА 1АГЗЮ Уб 16АГ СІЧАРЬ РжДй.
МіУтПыРИЗЮ 166АГ СІЧАРЬ ЧуАЁЕЧОњРИИч, Бз Сп 16АГ СІЧАРЬ FDA EUA(БфБоЛчПыНТРЮ) СІЧАРИЗЮ ЕюЗЯЕЧОю РжДй.
БЙГЛ ЙцПЊПЁМ ЛчПы СпРЮ БфБоЛчПы НТРЮЕШ ФкЗЮГЊ19 СјДмНУОрРК ‘КаРкСјДм(RT-PCR) ЙцНФ’РЛ ЛчПыЧЯДТ РЏРќРк СјДмНУОр СІЧАРИЗЮ, ЛчПыИёРћПЁ ЕћЖѓ ШЎСј АЫЛчПыАњ РРБо МБКА АЫЛчПыРИЗЮ БИКаЕШДй.
‘ШЎСјАЫЛч СІЧА’РК ФкЗЮГЊ19 АЈПАРкРЧ ШЎСјРЛ ИёРћРИЗЮ 6НУАЃ РЬГЛ АсАњИІ ШЎРЮЧЯПЉ СјДмЧв Мі РжДй.
‘РРБо МБКААЫЛч СІЧА’РК 1НУАЃ РЬГЛ АсАњИІ ШЎРЮЧв Мі РжДТ СІЧАРИЗЮ, БфБоЧб МіМњРЬ ЧЪПфЧб ШЏРк Ею СпСѕРРБоШЏРкИІ ДыЛѓРИЗЮ КќИЃАд ФкЗЮГЊ19 РНМКРЛ ШЎРЮЧЯДТ ИёРћРИЗЮ ЛчПыЧЯАэ РжНРДЯДй. ДйИИ, АЫЛч АсАњ ОчМКРЮ АцПь ‘ШЎСј АЫЛч СІЧА’РИЗЮ РчАЫЛчЧЯПЉ ШЎСјПЉКЮИІ ЦЧДмЧЯЕЕЗЯ ЧЯАэ РжДй.
НФОрУГДТ БЙГЛ ФкЗЮГЊ19 ЙцПЊШАЕППЁ ЛчПыЧЯДТ СјДмНУОрРЧ ЧАСњПЁ ДыЧб НХЗкЕЕИІ ГєРЬАэ ОШСЄРћРЮ АјБоУМАшИІ АЎУпАэРк ФкЗЮГЊ19 СјДмНУОрПЁ ДыЧб НХМгЧб СЄНФЧуАЁАЁ РЬЗчОюСњ Мі РжЕЕЗЯ СіПјЙцОШРЛ ИЖЗУЧЯПЉ НУЧрЧЯАэ РжДй.
ЧіРч, РЏРќРк СјДмНУОр(RT-PCR) Йз ИщПЊАЫЛч(ЧзПјАЫЛч, ЧзУМАЫЛч) Ею Уб 18АГРЧ ФкЗЮГЊ19 СјДмНУОр СІЧАРЬ РгЛѓРћ МКДЩНУЧшРЛ АХУФ СЄНФЧуАЁ*ИІ НХУЛЧЯПДАэ, РгЛѓРћ МКДЩНУЧшАшШЙ НТРЮРЛ ЙоРК 14АГ СІЧАРЬ МКДЩНУЧш СпПЁ РжДй.
ФкЗЮГЊ19 СјДмНУОрРК АЫУМ ГЛРЧ ЙйРЬЗЏНК РЏЙЋИІ ШЎРЮЧЯДТ ‘РЏРќРк СјДмНУОр(RT-PCR)’, ‘ЧзПјСјДмНУОр’Ањ АЫУМ ГЛРЧ ЙйРЬЗЏНКПЁ ДыЧб ЧзУМ РЏЙЋИІ ШЎРЮЧЯДТ ‘ЧзУМСјДмНУОр’ Ею 3СОЗљАЁ РжДй.
‘РЏРќРк СјДмНУОр’РК ШЏРкАЫУМ ГЛРЧ ЙйРЬЗЏНК РЏРќРкИІ СѕЦјЧЯДТ ‘КаРкСјДм(RT-PCR) ЙцНФ*’РИЗЮ, ЙйРЬЗЏНК РЏЙЋИІ ШЎРЮЧЯПЉ АЈПА ПЉКЮИІ СјДмЧеДЯДй. РЬ ЙцНФРК АњЧаРћРИЗЮ АЁРх СЄШЎЕЕАЁ ГєОЦ, ФкЗЮГЊ19 ШЎСјПыРИЗЮ ЛчПыЧЯАэ РжДй.
‘ЧзПј СјДмНУОр’РК ЙйРЬЗЏНКРЧ ЦЏСЄ ДмЙщСњРЛ РЮНФЧЯПЉ АЫУМГЛРЧ ЙйРЬЗЏНК РЏЙЋЗЮ АЈПА ПЉКЮИІ ШЎРЮЧеДЯДй. ДйИИ, КёРЮЕЮ‧БИРЮЕЮ Ею АЫУМИІ БзДыЗЮ ЛчПыЧЯПЉ ЙйРЬЗЏНКАЁ ЙЬЗЎРЮ АцПьДТ АЫЛч АсАњПЁ ПЕЧтРЛ Сй Мі РжДй.
‘ЧзУМ СјДмНУОр’РК ЙйРЬЗЏНК АЈПАПЁ ДыЧб ИщПЊЙнРРРИЗЮ ИИЕщОюСј ЧзУМРЧ Л§МК РЏЙЋИІ ШЎРЮЧЯДТ СІЧАРИЗЮ, ЧзУМАЁ Л§МКЕЧБт РЬРќРЮ УЪБт АЈПАДмАшПЁДТ РНМКРИЗЮ СјДмЕЩ Мі РжАэ АЫЛч ДчНУРЧ АЫУМ ГЛ ЙйРЬЗЏНК РЏЙЋИІ СїСЂРћРИЗЮ ШЎРЮЧЯБтПЁДТ ОюЗСПђРЬ РжДй.
БЙГЛ ЙцПЊПЁ ЛчПы СпРЮ ФкЗЮГЊ19 СјДмНУОрРЧ 1РЯ УжДы Л§ЛъЗЎРК Ор 16ИИИэКаРЬАэ, ЧіРчБюСі 359ИИИэКаРЛ Л§ЛъЧЯПЉ РЬСп 329ИИИэКаРЬ АјБоЕЧОњАэ(9.11. БтСи) СіБнБюСі Уб 212ИИАЧРЧ АЫЛч(СњКДАќИЎУЛ ХыАш)ИІ СјЧрЧпДй.
ЧіРч ШЎКИЕШ РчАэ Ор 30ИИИэКаРК УжБй РЯСжРЯ ЕПОШ 1РЯ ЦђБе АЫЛчЗЎ 1.5ИИИэКаРЛ АЈОШЧЯПДРЛ ЖЇ Ор 20РЯ АЃ РЧЗсЧіРхПЁ АјБоЧв Мі РжДТ ЙАЗЎРИЗЮ ОШСЄРћРЮ МіБоРЛ РЬОюАЁАэ РжДй.
ЧбЦэ, МіУтПы ФкЗЮГЊ19 СјДмНУОрРК ’20.8ПљБюСі 150ПЉАГ БЙАЁПЁ Уб 1Оя9,613ИИИэКаРЛ МіУтЧпДй.
СіГ 4Пљ 3,464ИИИэКаРЛ МіУтЧб РЬШФ 8ПљБюСі ИХПљ 3УЕИИИэКа РЬЛѓРЛ ГВОЦИоИЎФЋ, ЙЬБЙ Ею РќММАшЗЮ МіУтЧЯАэ РжДй.
БЙГЛ ФкЗЮГЊ19 СјДмНУОрОїУМДТ НХМгЧб АГЙп ДЩЗТРИЗЮ ММАшНУРхПЁ СјУтЧЯПЉ СІЧАРЧ ПьМіМКРЛ РЮСЄЙоОвАэ, БЙСІРћ РЇЛѓРЛ СіМгЧЯБт РЇЧи ГыЗТЧЯАэ РжДй.
ЧбЦэ ФкЗЮГЊ19‧ЕЖАЈ(РЮЧУЗчПЃРк) ЕПНУ СјДмНУОрРК 1АГ СІЧАРЬ РгЛѓРћ МКДЩНУЧшРЛ СјЧр СпРЬИч 10ПљБюСіДТ НФОрУГРЧ СЄНФЧуАЁИІ ЙоРЛ АЭРИЗЮ ПЙЛѓЧЯАэ РжДй.
НФОрУГДТ ФкЗЮГЊ19 СјДмНУОр ЛчПы‧АГЙп ЕПЧт ЕюРЛ СіМгРћРИЗЮ И№ДЯХЭИЕЧЯАэ, СОЛчРк БГРА АШИІ ХыЧи РќЙЎМК ЧтЛѓЧЯДТ Ею ЧАСњРЬ ПьМіЧб СІЧАРЬ АГЙпЕЧАэ НХМгШї ЧуАЁИІ ЙоРЛ Мі РжЕЕЗЯ РћБиРћРИЗЮ СіПјЧЯПЉ ПьИЎ БЙЙЮРЧ СјДм‧ФЁЗс БтШИИІ КИРхЧв Мі РжЕЕЗЯ УжМБРЛ ДйЧЯАкДйАэ ЙрЧћДй.
МлСјБИ БтРк webmaster@jybtv.kr
<РњРлБЧРк © РкРЏЙцМл, ЙЋДм РќРч Йз РчЙшЦї БнСі>

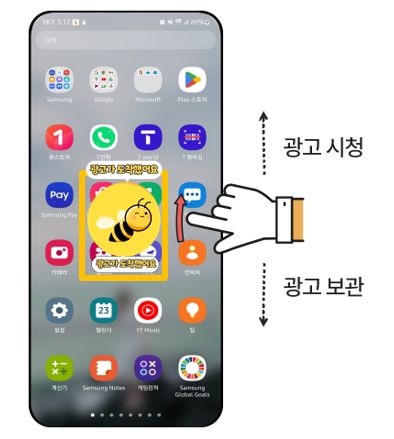 СжНФШИЛч ЁЎДѕ ОЦКёЁЏ, МвЛѓАјРЮ РЇЧб ЙЋЗсЦїРЮЦЎ ОюЧУ ЁЎОЦКёЁЏ УтНУ
СжНФШИЛч ЁЎДѕ ОЦКёЁЏ, МвЛѓАјРЮ РЇЧб ЙЋЗсЦїРЮЦЎ ОюЧУ ЁЎОЦКёЁЏ УтНУ